Aquestes darreres setmanes estem veient com el temps afecta el nostre dia a dia. I no, no estem parlant del trastorn afectiu estacional, sinó de la pluja que, per fi, ens acompanya. Són dies difícils per fer rentadores (el preu de la llum no ajuda), però encara més per eixugar la roba. Traiem l’entrellat de tot plegat: per què s’eixuga la roba?
Fem memòria: els canvis d’estat
En anteriors reportatges vam estar discutint les propietats de l’aigua i per què era una molècula tan important. Si seguíssim en aquesta línia, eventualment acabaríem parlant dels principals canvis d’estat de la matèria, representats a la següent imatge:
Així doncs, la roba mullada conté aigua en estat líquid entre les fibres tèxtils. La roba eixuta, en canvi, no conté aigua, cosa que sembla prou elemental. El nostre objectiu, en aquest cas, és passar aquesta aigua de l’estat líquid a l’estat gasós i que es perdi per l’atmosfera.
Et proposo un experiment mental: imagina que no tinguessis cap coneixement sobre eixugar la roba. Com dissenyaries un mètode per eixugar-la sabent que ha de passar d’estat líquid a estat gasós?
Jugant amb el diagrama de fases
Si parlem de canvis d’estat, cal considerar el diagrama de fases. Es tracta d’una representació que relaciona la pressió, la temperatura i els diferents estats de la matèria en què podem trobar una substància determinada. Per exemple, podem trobar diferents diagrames per representar l’aigua, el diòxid de carboni o el nitrogen.
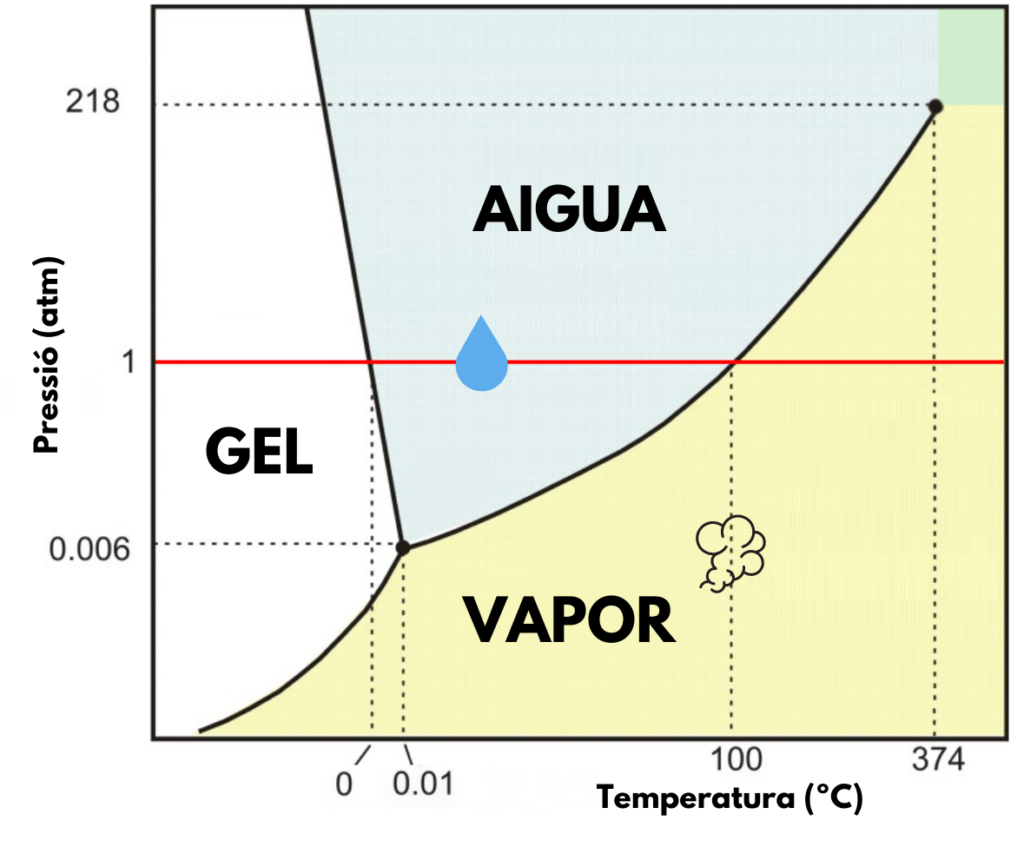
El nostre propòsit, doncs, a partir de les condicions estàndard de pressió (1 atmosfera) i temperatura (25 °C), és passar a la zona on l’aigua es troba en estat gasós. A priori, podríem considerar dues opcions: o bé augmentem la temperatura o bé disminuïm la pressió.
Per augmentar la temperatura, simplement podríem bullir l’aigua. Ficar la peça de roba en qüestió dins d’una olla i encendre els fogons. Però segurament, abans que l’aigua arribés als 100 °C, les fibres de la roba es farien malbé i hauríem malmès la nostra samarreta preferida.
Per disminuir la pressió, podríem introduir la samarreta en una cambra de buit, però la pèrdua de calor, la baixa efectivitat i la despesa energètica no compensarien les llargues estones que hauríem d’esperar per tenir la nostra roba eixuta.
Ebullició, evaporació, vaporització… quin embolic!
El secret, com sempre, està en els matisos. El nom genèric per portar una substància de l’estat líquid a l’estat gasós és la vaporització. Dins aquest procés, podem trobar dues variants: l’ebullició i l’evaporació.
Parlant en propietat, podem diferenciar els dos processos fàcilment a la cuina de casa nostra. L’ebullició és el procés que es dona en posar una olla amb aigua durant una bona estona al foc. En aquest moment, l’aigua assoleix la temperatura d’ebullició i fa la transició d’estat. Si, durant la preparació d’aquesta olla, ens hagués caigut una mica d’aigua a terra i no l’haguéssim fregat, al cap d’una estona no veuríem un bassal d’aigua: hi hauria hagut una evaporació tot i trobar-se a temperatura ambient, com és?
Avui, doncs, parlarem de l’evaporació (no portarem la roba a 100ºC). Per poder optimitzar el procés necessitem desgranar quins factors hi intervenen. Aquests són el tipus de líquid, la superfície lliure, la temperatura i la ventilació. Vegem-ne una breu explicació de cadascun!
Entenent l’evaporació
Per començar, ja hem vist que la temperatura és el factor que determina si hi ha ebullició o evaporació. D’entrada, la temperatura no és ni més ni menys que el moviment de les partícules. Així, la temperatura ambient ens permet determinar la quantitat d’energia que reben les molècules: com més temperatura, més energia i, per tant, més facilitat per escapar de la xarxa líquida i passar a l’estat gasós. Per visualitzar-ho, podríem comparar una bugada a l’hivern i una a l’estiu: oi que a l’estiu s’asseca més ràpidament?
Un altre concepte important és l’equilibri líquid-vapor. A la frontera entre les fibres tèxtils i l’aire que les envolta hi ha un balanç entre les molècules que es troben en estat líquid i aquelles que estan en estat gasós. D’entrada, aquest equilibri depèn molt del tipus de líquid, ja que algunes substàncies com l’acetona o l’etanol a temperatura ambient tenen un equilibri més desplaçat cap al gas i s’eixuguen més de pressa. També ho pots provar a casa: cronometra quant triga a desaparèixer una gota d’aigua i una gota d’acetona sobre una superfície seca!
Seguim! Aquest mateix equilibri també està condicionat per la superfície exposada de les fibres. Un manyoc de roba s’eixugarà més lentament que un llençol ben estès: això es deu al fet que les molècules que passen a estat gasós queden atrapades altre cop entre les fibres, condensant-se i tornant així a l’estat líquid. Com més estesa és la superfície, més fàcil el pas de líquid a gas.
I, finalment, tot i que mirem a nivell microscòpic la transició de l’aigua entre les fibres i l’aire que les envolta, tenim un efecte macroscòpic: la ventilació! El vent que pot estar bufant ens desplaça les molècules ja en estat gasós lluny de la roba, deixant espai perquè altres molècules en estat líquid ocupin el seu lloc. Així, s’accelera el procés de la mateixa manera que en un dia assolellat!
Amb aquesta informació, podem elaborar diferents experiments per comprovar l’efecte combinat dels diferents factors. Què contribueix més, la temperatura o la ventilació? Dit d’una altra manera, s’assecarà abans una samarreta en un dia tranquil d’estiu o en un dia ventós d’hivern?
Ja per acabar…
Un factor extern que no hem d’oblidar és el de la humitat, que podem descriure com la quantitat de vapor d’aigua present a l’aire. Per aquesta raó, ambients molt humits com el londinenc o el belga fan que efectes com la ventilació no tinguin tant de pes. L’alta humitat de l’aire provoca que no hi hagi un recanvi de molècules i, per tant, que s’hagin de crear estratègies per eixugar la roba.
És aquí on entren en joc aparells com els deshumidificadors o, senzillament, les assecadores. Aquestes darreres utilitzen ràfegues d’aire calent a pressió aprofitant els factors temperatura i ventilació que hem mencionat prèviament. I tot en qüestió de minuts!
Però si el que realment et preocupa és el temps que trigarà la bugada a eixugar-se, durant l’edició del 2019 de la Hackató de la UPC s’hi va presentar un projecte -amb participació de membres de Ciència Oberta– on l’aplicació Dry or Cry calculava el temps que trigaria la roba a estar eixuta tenint en compte la temperatura, el vent, la humitat relativa i la radiació solar segons la teva localització! Un parell de clics i ja sabràs quan et convé posar les agulles d’estendre.
Per saber-ne més
ScienceLab – Per què s’asseca la roba quan la pengem a l’ombra?
The Naked Scientist – How do clothes dry?
Conservation Physics – The physics of drying clothes
Imatge de portada: extreta del banc de fotografies de domini públic Pixabay
- Font pròpia
- Imatge adaptada a partir del blog “Un món de ciències ple de lletres” amb llicència Creative Commons 4.0
- Imatge extreta del banc de fotografies de domini públic Pixabay
- Font pròpia









Hola!
Buscant algun esquema que expliqués el canvi d’estat de la materia he topat amb la teva pàgina de divulgació a Ciència Oberta del 27 de març del 2022.
Fixa’t en l’imatge dels processos que permeten a la materia canviar d’estat: les fletxes que indiquen les accions entre l’estat sòlid i el líquid estan en la direcció equivocada.
Una errata involuntària de segur però que convindria corregir.
Gràcies per la vostra atenció.